|
 |
 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Главная >>> Гепатиты | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
ВведениеК настоящему времени накоплен большой опыт ведения и лечения пациентов с гепатитом С, который положен в основу представленных рекомендаций. Вирус гепатита С (ВГС) был открыт более двадцати лет назад. В настоящее время абсолютно очевидны серьезные проблемы, которые связаны с данной инфекцией: высокая частота формирования хронических форм, длительное бессимптомное течение, манифестация заболевания на поздних стадиях (цирроз печени), четкая ассоциация с развитием гепатоцеллюлярной карциномы. В результате проведения комплекса многоплановых профилактических мероприятий, в том числе в рамках национального приоритетного проекта в сфере здравоохранения, в Российской Федерации заболеваемость острым гепатитом С снижается, о чем свидетельствуют следующие данные: в 2011 году в России заболеваемость острым гепатитом С составила 1,8 на 100 тыс. населения, а в 2000 году - 22,2 на 100 тыс. населения. Всего в 2011 г. зарегистрировано 2613 больных острым гепатитом С (ОГС), протекавшим преимущественно в желтушной форме. Заболеваемость хроническим гепатитом С (ХГС) напротив увеличивается, в 2011 году этот показатель составил 39,9 на 100 тыс. населения (в абсолютных числах - это 57 028 человек), а в 2005 г, этот показатель составлял 32,0 на 100 тыс. населения. В общей структуре хронических вирусных гепатитов доля ХГС составила в 2012 году 74,4%. Кроме того, заслуживает внимания, что в 2011 году по данным официальной статистики в ряде регионов число лиц с наличием в крови антител к вирусу гепатита С (анти-ВГС) среди беременных женщин выросло в 3-5 раз по сравнению с 2000-2001 гг. Обращает на себя внимание, что среди регистрируемого в последние годы в Российской Федерации ХГС половину составляли лица младше 40 лет [19, 27-29]. Известно, что вирус гепатита С имеет 6 генотипов и большое число подтипов. В Российской Федерации распространены по убывающей частоте генотипы 1, 3, 2. Среди подтипов чаще встречается 1в, чем 1а, что аналогично европейской популяции, а также - 3а. Генотипы 4-6 практически не встречаются в популяции Российской Федерации. В структуре гепатита С отмечено увеличение числа больных с генотипом 3а. Выявлена значительная частота сочетания гепатита С с гепатитом В. Маркеры вируса гепатита В (ВГВ) обнаруживаются у пациентов с ХГС в 22% случаев, что делает обоснованной целесообразность вакцинации против ВГВ больных ХГС. Установлена низкая частота перинатальной передачи ВГС от матерей с ХГС родившимся у них детям (3,5%), в то время как у женщин с сочетанием ХГС с ВИЧ-инфекцией перинатальная передача ВГС составила 14-16% [5-7,21, 22, 24-26, 31] Рекомендации по диагностике и лечению пациентов с гепатитом С служат руководством для практических врачей, осуществляющих ведение и лечение таких пациентов на разных стадиях заболевания. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Рекомендации включают в себя следующие разделы:
Таблица 1. Уровни доказательности приводимых научных утверждений [33]
Скрининг на гепатит С [19, 30, 33-34]Кому рекомендуется скрининговое обследование на гепатит С (А-I)
Диагностика гепатита СЛабороторные исследованияС целью диагностики гепатита С и мониторирования пациентов с гепатитом C используются следующие лабораторные методики (А-1):
Исследование анти-ВГС в сыворотке крови должно выполняться лицам из выше перечисленных групп риска, а также пациентам с предполагаемым диагнозом острого или хронического гепатита С. В тех случаях, когда у пациентов в сыворотке крови определяются анти- ВГС (В-1) и/или им планируется противовирусное лечение необходимо исследование РНК ВГС высокочувствительным методом - (рекомендованная диагностическая чувствительность качественного исследования - 50 МЕ/мл и выше) (А-1). Пациентам с заболеванием печени неуточненной этиологии даже при отрицательном результате исследования анти-ВГС рекомендуется определение РНК ВГС; также этот тест целесообразно выполнять пациентам с иммунодефицитом, либо получающим иммуносупрессивную терапию Определение полиморфизма гена интерлейкина - 28ВВ последние годы доказана эффективность исследования полиморфизма гена ИЛ-28В как предиктора достижения УВО как при использовании двойной терапии пегилированным интерфероном/рибавирином, так и при проведении тройной терапии с включением ингибиторов протеазы у пациентов с генотипом 1 ВГС. Ген ИЛ28В, кодирующий интерферон лямбда 3-го типа, расположен на 19-й хромосоме. Высоким предсказательным значением в отношении достижения УВО обладает однонуклеотидный полиморфизм аллелей С (цитозин) или Т (тимин) в позиции rs12979860. Генотип СС приблизительно в 2 раза чаще встречается у пациентов со спонтанным клиренсом ВГС при остром гепатите С в сравнении с теми, у которых инфекция приобрела хроническое течение. Среди пациентов ХГС с генотипом 1 европеоидной расы, леченных пегилированным интерфероном/рибавирином и имеющих генотипы СС, СТ и ТТ устойчивый вирусологический ответ достигается в 69%, 33% и 27% соответственно. Предсказательное значение определения полиморфизма гена ИЛ-28В относительно достижения УВО на этапе планирования ПВТ выше предсказательной силы уровня вирусной нагрузки, стадии фиброза, возраста и пола пациента. Это служит основанием для включения данного теста в план обследования пациентов перед назначением ПВТ при генотипе 1 ВГС. Кроме того, результат анализа в гене ИЛ-28В полезен в отборе пациентов для назначения двойной схемы ПВТ с включением пегилированного интерферона/рибавирина или тройной схемы с включением одного из ингибиторов протеазы. В России в одном исследовании [12] получены
аналогичные данные о влиянии полиморфизма гена ИЛ-28В у пациентов с ХГС,
инфицированных генотипом 1 ВГС на результаты лечения стандартным Это дает основание рассматривать в случае необходимости (ограниченный экономический ресурс и показания для незамедлительного начала терапии) возможность проведения лечения стандартным интерфероном/рибавирином пациентов молодого возраста с генотипом 1 ВГС при условии выявления генотипа СС (полиморфизм rs12979860) гена ИЛ28В человека, низкой вирусной нагрузки, отсутствии сопутствующих заболеваний/состояний определяющих снижение эффективности противовирусной терапии (ожирение, инсулинорезистентность, стеатоз, фиброз печени 3 или 4 стадии) (С-2) Пункционная биопсия печениПункционная биопсия печени (ПБП) - широкодоступный и безопасный метод оценки морфологических изменений печени у пациентов ХГС. ПБП позволяет оценить локализацию и распространенность фибротического процесса и некровоспалительных изменений. Результаты ПБП легко интерпретируются и поддаются полуколичественной оценке. ПБП проводится в динамике с целью оценки прогрессирования поражения печени при ХГС. ПБП - единственный доступный метод, позволяющий оценить вклад сопутствующих заболеваний (стеатогепатит, гемохроматоз, аутоиммунный гепатит и т.д.) в патологическом процессе и их влияние на течение и эффективность лечения ХГС. Необходимо помнить, что ПБП имеет ряд ограничений. В частности, имеет значение :
ПБП, являясь «золотым стандартом» диагностики хронических гепатитов, требует строгого соблюдения правил ее выполнения в условиях специализированных отделений и наличия квалифицированных морфологов. Проведение ПБП требует соблюдения следующих правил:
Оценка результатов ПБП проводится с применением полуколичественных шкал описания степени некро-воспалительных изменений и стадии фиброза в ткани печени (Knodell, Ishak, METAVIR и т.д.- см. таблицы 3 и 4) [18,33-34]. Неинвазивная диагностика фиброза печениНа основании результатов исследований проведенных зарубежом и в России доказана диагностическая точность эластометрии (эластографии) и лабораторных тестов крови - ФиброТест и ФиброМетр V - в неинвазивной оценке стадий фиброза печени [9, 16-18, 32-34, 42]. Комбинация эластометрии и лабораторных тестов повышает точность оценки стадии фиброза. Эластометрия (эластография). Исследование проводится на аппарате «FibroScan» и позволяет судить об изменении эластических свойств печени на основании отраженных вибрационных импульсов и последующего их компьютерного анализа. Применение эластографии возможно на всех стадиях фиброза печени (F0- F4) у больных ХГС. К преимуществам метода относятся:
Интерпретация результатов
эластометрии затруднена в случаях:
Критерии успешного результата исследования:
ФиброТест (компонент диагностической панели Фибро-АктиТест и ФиброМакс) включает 5 не коррелирующих между собой биохимических показателей: α-2-макроглобулин, гаптоглоблин, аполипопротеин А1, гамма- глутамилтранспептидазу (ГГТП) и общий билирубин, которые позволяют оценивать выраженность фиброза с помощью дискриминантной функции. ФиброТест позволяет дифференцировать фиброз (F1-F3) от цирроза печени (F4) у пациентов ХГС. Интерпретация результатов ФиброТеста затруднена в случаях:
ФиброМетр (компонент диагностической панели ФиброМетр V) включает 5 показателей биохимического и клинического анализов крови: α-2-макроглобулин, ГГТП, мочевину, ПИ (%), тромбоциты, которые позволяют оценивать выраженность фиброза с помощью дискриминантной функции. ФиброМетр позволяет дифференцировать умеренный фиброз (F1-F2) от выраженного фиброза (F3) и от цирроза печени (F4) у пациентов с ХГС. Интерпретация результатов ФиброМетра затруднена в случаях:
Хронический гепатит С (В 18.2)Хронический гепатит С - хроническое заболевание печени, продолжающаяся более 6 месяцев, в основе которого лежит инфицирование и поражение печени вирусом гепатита С и манифестирующее морфологически некротическими, воспалительными и фибротическими изменениями печеночной ткани различной степени тяжести. Естественное течение ВГС-инфекцииВирус гепатита С - одна из наиболее частых причин хронических заболеваний печени. Диапазон исходов ВГС-инфекции широк и колеблется от минимального до тяжелого поражения печени, включая развитие цирроза печени (ЦП) и гепатоцеллюлярной карциномы (ГЦК). Выделен ряд факторов, которые могут оказывать отрицательное влияние на естественное течение гепатита С:
Через 20-30 лет после инфицирования ВГС вероятность развития ЦП колеблется в диапазоне от 4% до 45%. Прогрессирование фиброза печени имеет не линейный характер и длится, как правило, в течение 20-40 лет от момента инфицирования. У части больных этот процесс происходит чрезвычайно медленно. Диагноз хронического гепатита С (А-1)
Если у пациента в сыворотке крови определяется РНК ВГС на протяжении более 6 месяцев, то можно говорить о хроническом гепатите С. В том случаев, если у пациента зарегистрирован положительный тест на анти-ВГС, но РНК ВГС обнаружить не удается, оснований для диагноза ХГС недостаточно. Кроме того, нужно помнить о необходимости дифференциального диагноза ХГС с ОГС, который в 80% случаев протекает в безжелтушной форме. РНК ВГС может определяться в крови уже через 2 недели от момента заражения, еще до появления анти-ВГС; последние могут не выявляться в течение первых 8-12 недель. Дифференциальный диагноз ОГС и ХГС обязательно должен включать анализ клинических, биохимических и эпидемиологических данных, например, симптомы интоксикации и появление желтухи, высокий уровень АЛТ и АСТ, особенно в сочетании с данными о недавнем переливании крови, инъекционном введении наркотических средств или других факторах риска инфицирования. Следует помнить, что анти-ВГС и РНК ВГС могут выявляться в крови в различных сочетаниях, и это требует дополнительной оценки клинических данных (табл. 2). Таблица 2.
Сочетания маркеров вируса гепатита С в различных
Для формирования окончательного диагноза целесообразно, особенно при выявлении только одного из двух маркеров ХГС, проводить повторное тестирование анти-ВГС и РНК ВГС . Нередко ХГС протекает с нормальными значениями АЛТ и АСТ в сыворотке крови, риск прогрессирования заболевания печени у таких лиц представляется низким. Вместе с тем показано, что приблизительно у 25% пациентов с ХГС и нормальным уровнем сывороточных аминотрансфераз при проведении биопсии печени определяются признаки фиброза. Если у больного ХГС регистрируется постоянно повышенный уровень АЛТ и АСТ, то риск прогрессирования заболевания и развития его осложнений (в первую очередь - цирроза печени) существенно выше [31, 33, 34]. Морфологическая диагностика ХГС [9,18, 30, 33, 34]Данные, полученные при пункционной биопсии печени, позволяют определить стадию заболевания (степень выраженности фиброза), что имеет решающее значение в выборе лечебной тактики: врачебное решение о проведении противовирусной терапии или динамическое наблюдение за пациентом. Кроме того, при гистологическом исследовании определяется активность заболевания, а также могут быть обнаружены морфологическое признаки, потенциально влияющие на течение ХГС: стеатоз, избыточное накопление железа и т.д.. Как и всякий инвазивный метод, ПБП, являясь «золотым стандартом» диагностики хронических гепатитов, требует исполнения правил ее проведения в специализированных учреждениях и квалифицированного персонала для интерпретации результатов (см выше) Для интерпретации результатов ПБП используются полуколичественные шкалы определения активности патологического процесса в печени и фиброза (Knodell, Ishak, METAVIR - см. таблицы 3 и 4). Таблица 3. Морфологическая диагностика степени некровоспалительной активности гепатита
Таблица 4. Морфологическая диагностика стадии заболевания печени (выраженности фиброза)
Для определения стадии заболевания печени чаще применяется шкала. METAVIR. В последние годы предприняты и внедрены в клиническую практику неинвазивные методы оценки фиброза, прежде всего эластометрия, Информативность этих методов зависит от соблюдения правил их выполнения (см выше). Показания к проведению пункционной биопсии печени при хроническом гепатите С:
Выполнение ПБП не обязательно (решение принимает врач на индивидуальной основе) в следующих случаях:
Противовирусное лечение хронического гепатита СКритерии отбора пациентов для лечения [30, 33-34,40]Решение о назначении пациенту с ХГС противовирусной терапии должно быть индивидуализировано и основано на анализе следующих факторов:
Причинная связь между заболеванием печени и инфекцией ВГС должна быть доказана. Перед началом ПВТ необходимо оценить тяжесть поражения печени (стадию заболевания) и базовые вирусологические параметры (уровень вирусной нагрузки, генотип ВГС). Особого внимания требует стадия заболевания, поскольку жизненный прогноз и вероятность ответа на ПВТ у пациента с циррозом существенно отличаются от таковых у пациентов без ЦП. В связи с тем, что заболевание печени может прогрессировать у больных с постоянно нормальным уровнем АЛТ, оценка тяжести поражения печени должна проводиться без учета этого показателя. В настоящее время установить индивидуальный для пациента риск развития прогрессирующего заболевания печени невозможно, поэтому все пациенты с хроническим заболеванием печени (при компенсированной ее функции), этиологически связанным с ВГС, ранее не получавшие лечения, вне зависимости от исходной биохимической активности (уровень АЛТ, АСТ), должны рассматриваться, как кандидаты для проведения ПВТ (А2). Современные рекомендации определяют лишь сроки начала ПВТ в зависимости от степени морфологических изменений в ткани печени (стадии фиброза): а именно: можно или нельзя в настоящий момент времени отложить назначение ПВТ. Так пациентам с выраженным фиброзом (METAVIR F3-F4) показано незамедлительное начало ПВТ, пациентам с умеренным фиброзом (METAVIR F2) начало лечения очень желательно (В2). При менее выраженной степени фиброза, показания к ПВТ определяются индивидуально. Цель терапии - улучшение качества и продолжительности жизни пациентов с хроническим гепатитом С (профилактика прогрессирования заболевания в цирроз и ГЦК), что может быть достигнуто только при эрадикации вируса, что в клинической практике соответствует устойчивому вирусологическому ответу (УВО). УВО означает отсутствие РНК ВГС в крови через 24 недели после окончания терапии. После достижения устойчивого клиренса РНК ВГС прогрессия фиброза печени прекращается, что исключает развитие цирроза. Фиброз на доцирротической стадии (METAVIR < F3) может регрессировать. Риск развития ГЦК устраняется у пациентов без цирроза. Снижается, но не исчезает полностью, у пациентов с ЦП. Двойная терапия хронического гепатита С (пегилированный интерферон α-2а или α-2b в сочетании с рибавирином)Оценка эффективности противовирусной терапии. Для оценки эффективности и, возможно, последующей модификации ПВТ используется определение РНК ВГС после 4, 12, 24 неделе терапии, а также через 24 недели после ее окончания. Для характеристики вирусологического ответа может быть использована следующая терминология:
Здесь и далее: Определение и количественную оценку РНК ВГС следует проводить с помощью чувствительного метода (нижний предел обнаружения не менее 50 МЕ/мл), а уровни РНК ВГС следует выражать в МЕ/мл (С1) Предикторы благоприятного ответа на противовирусное лечение ХГС:
Стандартные схемы противовирусной терапииПегилированный интерферон α-2а или α-2в, в сочетании с рибавирином рассматриваются в качестве терапии первой линии у пациентов с ХГС. Инъекции ПЭГ-ИФН α проводятся один раз в неделю подкожно, в то время как Рибавирин назначается ежедневно перорально. Схема дозирования пегилированного интерфернона: ПЭГ-ИФН α2а 180 мкг/нед , ПЭГ-ИФН α 2в из расчета 1,5 мкг/кг/нед Схема дозирования рибавирина:
Длительность терапии определяется генотипом: для генотипа 1 и 4 она составляет 48 недель, для генотипов 2 и 3 - 24 недели. Однако, согласно современным рекомендациям по ведению и лечению пациентов с ХГС с использованием принципов «терапии согласно вирусологическому ответу» (Response Guide Therapy) длительность стандартного лечения может быть изменена - см. таблицы 4 и 5. Таблица 5. Длительность противовирусного лечения при генотипах 1 и 4 в соответствии с принципом «терапия согласно вирусологическому ответу»
Здесь и далее: фармакотерапевтические характеристики указанных в «Рекомендациях...» лекарственных средств см. Инструкцию производителя Таблица 6. Длительность противовирусного лечения при генотипах 2 и 3, в соответствии с принципом «терапия согласно вирусологическому ответу»
Исследования, которые необходимо выполнить пациентам до начала противовирусной терапииПомимо вирусологических тестов (определение уровня РНК ВГС, генотипа ВГС), определения стадии заболевания печени (выполнение биопсии печени или применение методов неинвазивной диагностики фиброза) пациент - кандидат для проведения ПВТ должен быть обследован для исключения сопутствующих заболеваний с тем, чтобы обеспечить максимальную эффективность и безопасность проводимой терапии (табл. 7). Таблица 7. План обследования пациента перед началом противовирусной терапии
Наблюдение за пациентами в процессе противовирусного лечения (А-1)Наблюдение за пациентами в процессе ПВТ включает в себя два аспекта:
Вирусологический ответ отражает эффективность проводимой терапии (см выше). РНК ВГС необходимо исследовать
Параллельно с РНК ВГС в те же временные точки пациенту исследуется АЛТ с целью определения биохимического ответа. Для контроля над нежелательными явлениями необходимо соблюдать график посещения врача пациентом:
В случае необходимости пациент может посещать врача чаще, что решается на индивидуальной основе. При каждом посещении врача необходим расспрос и осмотр пациента с целью контроля над развитием нежелательных явлений (гриппоподобный синдром, кожные элементы - сыть, гиперемия в местах инъекций интерферона и т.д.) При каждом плановом посещении врача пациент должен заполнять шкалу Бека с целью контроля над возможностью развития депрессии. Исследование клинического анализа крови с подсчетом абсолютного числа нейтрофилов, определением уровня гемоглобина, количества эритроцитов и тромбоцитов необходимо выполнять
Это связано с тем, что наиболее частыми гематологическими побочными действиями проводимого лечения являются нейтропения, анемия и тромбоцитопения. В период ПВТ пациенту необходимо исследовать уровень ТТГ и свободного тироксина каждые 3 месяца. В период ПВТ и последующих 24 недель наблюдения пациенты должны соблюдать контрацепцию двумя методами, один из которых барьерный, в связи с возможными тератогенными свойствами рибавирина. Коррекция дозы/прекращение лечения при использовании двойной схемы ПВТВ настоящее время четко определены показания для изменения дозы препаратов и прекращения лечения вследствие ожидаемых побочных действий (нежелательных явлений). Так, снижение дозы пегилированного интерферона необходимо при развитии следующих побочных эффектов:
Дозу пегилированного интерферона рекомендуется снижать ступенчато:
Если у пациента диагностируется депрессия Депрессия оценивается по шкале Бэка (приложение 2) на каждом визите, при этом:
Отмена пегилированного интерферона целесообразна при уменьшении абсолютного числа нейтрофилов ниже 500/мм, снижения уровня тромбоцитов менее 25 000/мм. В последующем в случае увеличения числа нейтрофилов и тромбоцитов лечение может быть возобновлено с применением более низкой дозы пегилированного интерферона. Уменьшение дозы Рибавирина (на 200 мг) необходимо при снижении уровня гемоглобина менее 100 г/л. Прекратить прием рибавирина следует при снижении уровня гемоглобина до 85 г/л и менее.
В качестве альтернативной лечебной тактики для сохранения дозы противовирусных препаратов могут быть применены факторы роста, назначение которых врачом выполняется на основании индивидуальных особенностей каждого пациента. Пациенты, с неудачным опытом ПВТ пегилированным интерфероном в сочетании с рибавирином (не достигшие УВО) Генотип 1: учитывая невысокий процент достижения УВО (10-15 %) у пациентов неответивших на предыдущий курс ПВТ, а также у пациентов с рецидивом или вирусологическим прорывом, следует воздержаться от проведения повторных курсов стандартной двухкомпонентной схемы терапии пегилированным интерфероном/рибавирином (А2). Эти пациенты - кандидаты для проведения тройной противовирусной терапии с включением прямых противовирусных препаратов (см. ниже). При неотложных показаниях и/или при наличии данных о недостаточно адекватном предыдущем курсе терапии, в отсутствие прямых противовирусных препаратов, возможно рассмотрение вопроса о проведении повторного курса ПВТ двойной схемой. Все генотипы кроме 1-го: при наличии показаний, в отсутствие противопоказаний возможно проведение повторного курса ПВТ ПЭГ-ИФН α в сочетании с Рибавирином. Прямые противовирусные препараты - ингибиторы протеазы вируса гепатита С первого поколения применяются только у пациентов с 1-м генотипом ВГС. Поддерживающая терапия низкими дозами интерферона с целью снижения риска прогрессирования заболевания и развития ГЦК не доказала своей эффективности и не рекомендуется в настоящее время, в том числе и пациентам с ЦП (А2). Стандартный интерферон α в сочетании с рибавирином в лечении хронического гепатита СВ России применяется также комбинированная терапия ХГС стандартным интерфероном α (3 млн МЕ 3 раза в неделю в\м или п\к) в сочетании с рибавирином (из расчета по массе тела, как указано выше при описании режима лечения с включением пегилированного интерферона α - 15 мг/кг массы тела пациента). Однако необходимо учитывать, что эффективность такой схемы лечения ниже, чем при применении пегилированного интерферона α в сочетании с рибавирином. Тем не менее, в условиях ограниченного экономического ресурса, на основании полученного в России опыта [1,2,10,14,15] этот вид ПВТ может применяться, следуя принципу «терапия согласно вирусологическому ответу» (аналогично ПВТ пегилированным интерфероном α/рибавирином) для особой группы пациентов:
При соблюдении описанных выше условий частота УВО составляет 84 - 94%. Правила наблюдения за пациентами в процессе ПВТ стандартным интерфероном α/рибавирином аналогичны таковым для пегилированного интерферона α/рибавирина. Побочные эффекты (нежелательные явления) леченияОбщая частота побочных эффектов, вследствие которых лечение должно быть прекращено, составляет 10-14%. Наиболее распространены гриппоподобные симптомы (слабость, головная боль, температура) и психиатрические нарушения (депрессия, раздражительность, бессонница), которые отмечаются у 22-31 % пациентов. Среди лабораторных изменений наиболее часто встречается нейтропения (18-20%). При выраженном снижении количества нейтрофилов, инфекционные осложнения крайне редки, поэтому применение гланулоцитарных колониестимулирующих факторов показано лишь в отдельных случаях. При развитии психиатрической симптоматики показана консультация психиатра. Пегилированные интерфероны могут индуцировать развитие аутоиммунных заболеваний (аутоиммунный тиреоидит) или ухудшать течение имевшихся до назначения ПВТ аутоиммунных расстройств. Необходимо различать пациентов, у которых гепатит С протекает с чертами аутоиммунного гепатита (показано противовирусное лечение) и пациентов с первичным аутоиммунным гепатитом, на фоне которого развился гепатит С. В последнем случае при наличии у пациента двух сочетанных заболеваний- аутоиммунного гепатита и хронического гепатита С показана иммунносупрессивная терапия. Наиболее частым побочным эффектом рибавирина является гемолитическая анемия. Модификация дозы рибавирина требуется у 9-15% пациентов. Эритроцитарные факторы роста (эритропоэтин) несколько улучшают самочувствие больных и уменьшают необходимость в снижении дозы рибавирина, но их благоприятное влияние на частоту достижения УВО доказано не было, а безопасность окончательно не установлена. Их применение, хотя и редко, может сопровождаться такими побочными эффектами, как тромбоэмболия, красноклеточная аплазия, прогрессирование ряда онкологических заболеваний и смерть. На сегодняшний день применение факторов роста на фоне комбинированной противовирусной терапии гепатита С не может быть рекомендовано к широкому практическому использованию. Предпочтительным методом коррекции цитопений остается модификация дозы соответствующих препаратов. Поскольку рибавирин выводится через почки, необходимо соблюдать осторожность при назначении его пациентам с почечной патологией. Рибавирин обладает тератогенным действием, поэтому на протяжении лечения и в течение 6 месяцев после его завершения необходимо избегать наступления беременности. Мужчинам, чьи партнерши беременны, лечение рибавирином также не проводится. Наблюдение за пациентами, завершившими курс противовирусной терапии (А-1)Пациенты, достигшие УВО после курса противовирусной терапии, без цирроза печени должны быть повторно обследованы через 48 недель после окончания терапии, а затем еще раз через год с определением у них уровня АЛТ и РНК ВГС в крови. Если уровень АЛТ остается в пределах нормальных значений, а тест на РНК ВГС отрицателен, то можно считать, что пациент вылечен от гепатита С. Поскольку даже после завершения ПВТ у пациентов может развиться гипотиреоз, уровень ТТГ и свободного тироксина пациентам необходимо исследовать через год после завершения ПВТ. Пациенты с ЦП даже в случае достижения УВО в результате противовирусного лечения должны оставаться под наблюдением врача: методом ЭГДС необходимо контролировать состояние вен пищевода каждые 1 -2 года, скрининг ГЦК необходимо проводить 1 раз в 6 месяцев с проведением УЗИ печени и определением уровня АФП. Противопоказания к противовирусной терапии гепатита СК противопоказаниям для назначения интерферона/пегилированного интерферона относят
Относительными противопоказаниями к назначению ПВТ считаются
Пациенты с ЦП и количеством баллов <7 по классификации Чайлд-Пью должны проходить лечение в медицинских учреждениях, имеющих опыт ведения таких пациентов, а его безопасность и эффективность особенно тщательно мониторироваться. Тройная терапия хронического гепатита С с включением ингибиторов протеазы [33, 34, 36-38, 40-41,43]В настоящее время закончены исследования III фазы по изучению эффективности и безопасности тройной терапии с включением ингибиторов протеазы телапревира и боцепревира. Ингибиторы протеазы (телапревир или боцепревир) применяются только в комбинации с препаратами пегилированного интерферона и рибавирином и только у пациентов с генотипом 1 ВГС, как ранее нелеченных, так и имевших неудачный опыт терапии двойной схемой (пегилированным интерфероном/рибавирином). Лечение проводится по принципу “терапия согласно вирусологическому ответу”. Эффективность тройной схемы выше в сравнении со стандартной двойной терапией пегилированным интерфероном/рибавирином. При включении в схему лечения ХГС телапревира УВО составляет
При включении в схему лечения ХГС боцепревира УВО составляет
Лечение ХГС у пациентов с 1 генотипом вируса, ранее не получавших ПВТ, по тройной схеме с включением телапревираТелапревир назначается вместе с пегилированным интерфероном α-2а или α-2в и
рибавирином в течение 12 недель в дозе 750 мг три раза в день, каждые 7
- 9 часов вместе с едой. Пища должна содержать достаточное количество
жиров (20г). Далее в течение еще 12 - 36 недель
пациентам назначается только пегилированный интерферон и рибавирин Доза пегилированного интерферона и рибавирина рассчитывается аналогично тому, как это делается в процессе лечения ХГС двойной схемой:
Длительность ПВТ с включением телапревира может составлять 24 недели в тех случаях, когда у пациента нет цирроза печени, а уровень РНК ВГС не определяется на 4-й и 12-неделях (т.е. достигается продленный вирусологический ответ).
Для пациентов с циррозом печени длительность ПВТ с включением телапревира составляет 48 недель:
Прекращение лечения Лечение прекращается, если в процессе лечения тройной схемой с
включением телапревира уровень РНК ВГС составляет >1000 МЕ/мл после 4
или 12 недель. Следует отметить, что в этом случае отменяются все
противовирусные препараты (телапревир, пегилированный интерферон Пациентам, которым назначен 48-недельный курс лечения,
следует прекратить терапию пегилированным интерфероном и рибавирином в
том Продолжение терапии в этих условиях сопровождается крайне низкой вероятностью достижения УВО и способствует селекции резистентных штаммов вируса гепатита С (В-2). Лечение ХГС у пациентов с 1 генотипом вируса, ранее не получавших ПВТ, по тройной схеме с включением боцепревираБоцепревир (если препарат доступен) назначается в течение 24 - 44 недель в дозе 800 мг три раза в день (каждые 7-9 часов вместе с едой) в комплексе с пегилированным интерфероном α-2а или α-2в и рибавирином. Этому лечению предшествует 4-х недельный вводный период в течение которого пациенты получают только пегилированный интерферон и рибавирин (А-1). Доза пегилированного интерферона и рибавирина рассчитывается аналогично тому, как это указано выше при описании двухкомпонентной терапии. Для пациентов без цирроза печени тройная терапия с включением боцепревира начинается с 4-х недельного вводного периода применения пегилированного интерферона и рибавирина. Затем к терапии добавляется боцепревир. Если через 8 недель терапии РНК ВГС не определяется, длительность курса лечения может быть сокращена и составляет 28 недель, включая вводный период. Если через 8 недель лечения РНК ВГС определяется, тройная терапия проводится до 28 недель лечения (согласно дизайну исследования SPRINT2), затем боцепревир отменяется и до 48 недель продолжается терапия пегинтерфероном и рибавирином (В-2). Курс лечения по тройной схеме (с включением боцепревира) для пациентов с циррозом печени составляет 48 недель, включая 4 недели вводного периода терапии пегинтерфероном и рибавирином (В-2). Прекращение терапии с включением боцепревира необходимо в том случае, если уровень РНК ВГС составляет ≥ 100 МЕ/мл на 12-й неделе лечения либо определяется в любой концентрации на 24-й неделе лечения. Следует отметить, что прекращение лечения тройной схемой подразумевает отмену всех трех препаратов: боцепревира, пегилированного интерферона и рибавирина (В-2). Принципы применения тройной схемы ПВТ у ранее нелеченных пациентов с ХГС обобщены в таблице № 8. Таблица 8. Рекомендации по применению ингибиторов протеазы ВГС у
пациентов с ХГС, генотипом 1, ранее не получавших противовирусную
терапию [38 с изменениями]
Лечение ХГС у пациентов с генотипом 1, имеющих опыт неудачи противовирусной терапии интерфероном или пегилированным интерфероном в сочетании с рибавирином (без достижения УВО)Тройная схема с включением боцепревира или телапревира в дополнение к пегилиронному интерферону и рибавирину может быть успешно использована для повторного лечения пациентов, не достигших УВО в результате двойной терапии с включением интерферона или пегилированного интерферона в сочетании с рибавирином. Однако, эта тактика применима к тем пациентам, у которых на фоне ранее проведенной двойной терапии отмечался или рецидив ХГС или частичный вирусологический ответ (определения различных типов вирусологического ответа см выше) (A-1) Повторное лечение тройной схемой с включением телапревира в дополнение к пегилиронному интерферону и рибавирину может быть успешно проведено у пациентов с полным отсутствием ответа на ранее проведенную терапию интерфероном или пегилированным интерфероном в сочетании с рибавирином (В-2). Принцип “терапия согласно вирусологическому ответу” может быть применен при назначении тройной схемы с включением или телапревира (для пациентов с рецидивом), или боцепревира (для пациентов с рецидивом или частичным ответом на ранее назначавшуюся двойную терапию), но не для пациентов с полным отсутствием ответа. Отмена всех препаратов в тройной схеме с боцепревиром для пациентов с опытом ранее проведенной ПВТ без достижения УВО выполняется в том случае, если уровень РНК ВГС составляет > 100 МЕ/мл через 12 недель лечения (сопряжено с селекцией резистентных штаммов вируса) или определяется через 24 недели лечения (В-1). Отмена всех препаратов
в тройной схеме с телапревиром для пациентов с опытом ранее проведенной
ПВТ без достижения УВО осуществляется в том случае, если уровень РНК ВГС
составляет > 1000 МЕ/мл на 4-й или 12-й неделе лечения (сопряжено с
селекцией резистентных штаммов вируса) Лечение тройной схемой с другим ингибитором протеазы не проводится. Правила ведения пациентов ранее не ответивших на интерферон или пегилированный интерферон в сочетании с рибавирином на фоне лечения тройной схемой с включением телапревира или боцепревира обобщены в таблице 9. Таблица 9. Правила ведения пациентов ХГС с генотипом 1, на
фоне лечения тройной схемой с включением телапревира или боцепревира,
ранее не ответивших на интерферон или пегилированный интерферон в
сочетании с рибавирином [38 с изменениями]
Побочные действия тройной терапииАнемия, развивающаяся у пациентов на фоне назначения тройной терапии (более выражена при назначении боцепревира), корректируется снижением дозы рибавирина (правила снижения дозы рибавирина см выше). Аноректальные симптомы у пациентов на фоне лечения телапревиром корректируются применением топических кортикостероидов, антигистаминных препаратов и лидокаина. Сыпь и зуд на фоне применения телапревира должны оцениваться по площади распространения, при необходимости следует обратиться за консультациями к дерматологу (таблица 10, приложение 3) Таблица 10. Классификация нежелательных кожных явлений по
степени их тяжести и рекомендации по ведению больных
Лекарственное взаимодействиеТелапревир относится к препаратам-субстратам и ингибиторам цитохрома Р450 (СYР)3А4 а также трансмембранного переносчика Р-гликопротеина (Р-gр). Боцепревир может проявлять себя как субстрат цитохрома Р450 3A4/5, Р-gр и альдо-кеторедуктазы 1С2/1С3, а также как индуктор цитохрома Р4503A4/5. Вследствие особенностей фармакодинамики ингибиторов протеазы, назначение телапревира (также как и боцепревира) противопоказано одновременно с приемом целого ряда лекарственных препаратов, особенно тех, клиренс которых зависит от цитохрома Р450 3A (для телапревира) или цитохрома Р450 3A4/5 (для боцепревира) (таблица 11) [11]. Таблица 11. Лекарственные препараты, несовместимые с телапревиром и боцепревиром [11]
Острый гепатит С [30-33, 34]Острый гепатит С (В17.1) - вирусный гепатит с парентеральным механизмом передачи возбудителя - вируса гепатита С, характеризующийся высокой частой формирования хронических форм болезни (50-80%) и возможностью последующего развития у части больных цирроза печени и гепатоцеллюлярной карциномы. Острый гепатит С диагностируют на основании:
Особенную диагностическую ценность для установления диагноза ОГС имеет обнаружение анти-ВГС в динамике болезни (через 4-6 недель) при отрицательном результате исследования этого маркёра в ранние сроки болезни, а также исключение гепатита иной природы. Наличие РНК ВГС в фазе «серологического окна» (в период отсутствия анти-ВГС) является важным критерием диагноза среди комплекса диагностических признаков ОГС. Интерпретация различных маркеров при инфекции вирусом гепатита С представлена в таблице 2. Большинство пациентов с ОГС не демонстрируют каких-либо симптомов заболевания, у значительной части из них наступает спонтанная элиминация вируса, с которой ассоциируются следующие факторы:
Однако ни один из этих параметров не может лечь в основу предсказания характера течения заболевания у конкретного пациента. Подозрение на острый вирусный гепатит требует дифференциального диагноза, основные лабораторные показатели, которые необходимо исследовать, указаны в таблице 12. Таблица 12. Перечень основных лабораторных тестов для верификации диагноза при подозрении на острый вирусный гепатит
Показанием для проведения противовирусной терапии является ОГС с подтверждением виремии. Своевременно начатое лечение может сопровождаться развитием УВО более чем у 90% больных ОГС (В2). Подобная закономерность отмечается как при назначении «коротких», так и пегилированных интерферонов. На основании накопленных к настоящему времени данных, рекомендации по специфическому лечению больных ОГС, вне зависимости от генотипа вируса С можно свести к следующему:
Базисная терапия острого гепатита С включает:
Пациенты с выраженным фиброзом и циррозом печениПациенты с выраженным фиброзом (F3 METAVIR) и компенсированным ЦП при отсутствии противопоказаний рассматриваются в качестве кандидатов для незамедлительного начала противовирусной терапии по двойной или тройной схеме (если доступны ингибиторы протеазы), что в случае достижения УВО сопровождается достоверным уменьшением риска развития декомпенсации функции печени и ГЦК, повышением вероятности обратного развития фиброза (А-1) Частота достижения УВО у больных с выраженным фиброзом и циррозом печени несколько меньше в сравнении с частотой УВО у пациентов с F ≤ 2. В процессе проведения ПВТ эти пациенты должны более часто и тщательно наблюдаться. По индивидуальным показаниям в случае развития цитопений у них могут быть применены факторы роста (гранулоцитарный колониестимулирующий фактор роста для увеличения числа нейтрофилов, эритропоэтин в случае развития анемии, тромбоцитарный фактор роста в случае развития тромбоцитопении). Правила дозирования препаратов, продолжительность как двойной, так и тройной терапии указаны выше в соответствующих разделах. Скрининг ГЦК у пациентов с циррозом печени проводится 1 раз в 6 месяцев с определением уровня АФП и проведением УЗИ печени даже в тех случаях, когда ПВТ проведена успешно и УВО достигнут (B-1). ПВТ на основе применения пегилированного интерферона противопоказана пациентам с циррозом печени и количеством баллов по Чайлд-Пью более 7 в связи с риском развития декомпенсации функции печени. Тактика ведения пациентов с сочетанной инфекцией ВИЧ/ВГС [4, 30, 33-34]
Исследование на РНК ВГС необходимо проводить не только пациентам с выявленными анти-ВГС, но также тем, у кого в отсутствие анти-ВГС определяется повышенный уровень АЛТ. При впервые выявленной ВГС-инфекции рекомендуется провести определение стадии фиброза печени (пункционную биопсию печени или эластметрию или лабораторные тесты крови). В настоящее время проведение пункционной биопсии печени не обязательно у больных с большой вероятностью достижения УВО:
Назначение терапии ХГС больным ВИЧ-инфекцией зависит от числа CD4+ лимфоцитов. При количестве CD4+ лимфоцитов более 500 клеток/мкл рекомендуют начинать терапию только ХГС. При снижении числа CD4+ лимфоцитов менее 500 клеток/мкл рекомендуют начать АРВТ (антиретровирусную терапию) одновременно с терапией ХГС. Было доказано уменьшение прогрессирования фиброза печени на фоне восстановления иммунитета вследствие подавления репликации ВИЧ. При количестве СD4+ лимфоцитов менее 350 клеток/мкл начинают лечение ВИЧ-инфекции, а затем присоединяют терапию ХГС. Следует избегать назначения диданозина. Если возможно, не следует включать ставудин и зидовудин в схему АРВТ при одновременном лечении ХГС и ВИЧ-инфекции. При обнаружении стадии фиброза 0-1 у пациентов с сочетанной инфекцией ВИЧ/ВГС лечение может быть отложено вне зависимости от генотипа вируса гепатита С, особенно у пациентов с низкой вероятностью ответа на существующие в настоящее время режимы терапии, в первую очередь, с 1-м генотипом ВГС. Таким пациентам следует регулярно наблюдаться для динамического контроля выраженности фиброза. Стандартная терапия ХГС проводится у больных с ВИЧ-инфекцией при следующих условиях:
При стандартной терапии используются ПЭГ-ИФН- α-2а в дозе 180 мкг или ПЭГ-ИФН-α-2b в дозе 1.5 мкг/кг веса пациента подкожно раз в неделю. Рибавирин назначается в зависимости от массы тела больного (при весе больного 75 кг и меньше - 1000 мг/сутки; при весе более 75 кг - 1200 мг/сутки) внутрь ежедневно в два приёма. Оптимальная схема терапии представлена в приложении 4. Тактика ведения ВИЧ-инфицированных пациентов с впервые выявленным ХГС (генотип 1 ВГС)В случае определения стадии фиброза 0-1 решение о начале терапии ХГС принимается индивидуально:
В случае определения стадии фиброза 2-4 рекомендуют терапию ХГС ПЭГ-ИФН/Рибавирин с ингибитором протеазы ВГС. Первые пилотные исследования тройной терапии ХГС у больных ВИЧ- инфекцией препаратами с прямым противовирусным действием (телапревир и боцепревир) показали достоверно более высокий уровень УВО при сравнении с результатами двойной терапии. Телапревир (если это доступно) в дозе 750 мг три раза в день добавляют к основной двойной схеме терапии ХГС на 12 недель лечения. Если через 4 недели лечения РНК ВГС определяется в количестве менее 1000 МЕ/мл - терапию продолжают далее до 12 недель. При обнаружении РНК ВГС более 1000 МЕ/мл - отменяют всю терапию данному пациенту. Если через 12 недель терапии РНК ВГС выявляется в количестве менее 1000 МЕ/мл - продолжают двойную терапию ХГС до 24 недель. При отрицательных результатах обследования РНК ВГС спустя 24 недели терапию продолжают ещё 24 недели - всего 48 недель лечения. Если через 24 недели терапии ХГС продолжает выявляться РНК ВГС - лечение рекомендуют прервать. В отличие от пациентов с моноинфекцией ВГС, данных для сокращения курса терапии ХГС у больных ВИЧ-инфекцией пока недостаточно. Безопасность телапревира изучена при одновременном его назначении на фоне АРВТ, включавшей реатаз, ралтегравир, рилпривирин, этравирин, тенофовир, абакавир, эмтрицитабин, эпивир и эфавиренз (дозу телапревира увеличивают до 1125 мг три раза в сутки при одновременном приёме эфавиренза). Боцепревир (если это доступно) добавляют в дозе 800 мг три раза в день внутрь через 4 недели после начала основной двойной схемы терапии ХГС. В случае, если через 12 недель лечения выявляется РНК ВГС в количестве 100 МЕ/мл и более или обнаруживается на 24 неделе терапии - всю терапию ХГС отменяют. При уровне РНК ВГС менее 100 МЕ/мл через 12 недель лечения и отрицательных результатах обследования через 24 недели лечения - терапию продолжают до 48 недель. Безопасность боцепревира изучена при одновременном его назначении на фоне АРВТ, включавшей ралтегравир, этравирин, тенофовир, абакавир, эмтрицитабин, эпивир. Использование в терапии ХГС у больных ВИЧ-инфекцией препаратов с прямым противовирусным действием (телапревир и боцепревир) ассоциировано с более высоким риском развития нежелательных явлений лечения, особенно более частым развитием анемии, сыпи, анального зуда и извращения вкуса. Это требует более частого контроля уровня гемоглобина в течение первых недель терапии. Снижение дозы рибавирина является в данном случае эффективной мерой, не влияющей на частоту достижения УВО. Тактика ведения ВИЧ-инфицированных пациентов с впервые выявленным острым гепатитом С Рекомендуется определить количество РНК ВГС при установлении диагноза и спустя 4 недели. Одной из возможных схем лечения является назначение пегилированного интерферона в сочетании с рибавирином. Лечение начинают, если уровень РНК ВГС не снизился более 2 log10 спустя 4 недели от момента выявления РНК ВГС и/или продолжает выявляться через 12 недель наблюдения. Длительность курса зависит от достижения БВО: при достижении БВО длительность курса терапии составляет 24 недели, при отсутствии БВО - длительность лечения составляет 48 недель. Однако, при отсутствии снижения уровня РНК ВГС более log10 к 12 неделе лечения - терапию отменяют. Результатов рандомизированных исследований о длительности курса и роли рибавирина в терапии острого гепатита С недостаточно, также как и данных об использовании препаратов с прямым противовирусным действием. Поэтому, использование телапревира и боцепревира в терапии острого гепатита С у пациентов с ВИЧ-инфекцией не рекомендуется. Однако, при неэффективности проводимой терапии (отсутствие снижения уровня РНК ВГС более 2 log10 к 12 неделе лечения) их применение может быть рассмотрено в индивидуальном порядке. Тактика ведения пациентов с сочетанной инфекцией ВИЧ/ВГС, не ответивших на предыдущую терапию ХГС
Лечение особых групп пациентов и пациентов с сопутствующими заболеваниями [30, 33, 34]Употребление алкоголя
Употребление психоактивных веществ
Другие сопутствующие заболевания и состояния Необходим тщательный сбор анамнеза, обращая особое внимание на те факторы, которые усугубляют поражение печени. Трансплантация печени при циррозе печени ВГС-этиологииПациенты с терминальной стадией ЦП в исходе вирусных гепатитов составляют до 45% в Листах ожидания трансплантации печени (ТП). В лист ожидания ТВ включают пациентов с классами В и С по шкале Чайлд-Пью, большую часть из них составляют больные с циррозом печени ВГС- этиологии, меньшую - пациенты с ЦП ВГВ или ВГВ/ВГД-этиологии. Все пациенты в листах ожидания на ТП должны быть вакцинированы против гепатита А, пациенты с циррозом печени ВГС-этиологии должны быть вакцинированы против гепатита В. Вакцинация может быть проведена по «быстрой» или стандартной схеме в зависимости от степени неотложности оперативного лечения. Наличие репликации вируса гепатита С в крови пациента не является противопоказанием для трансплантации печени. Реинфекция трансплантата вирусом гепатита С после ТП развивается в 100% случаев (возвратная ВГС- инфекция). Фиброз в трансплантате на фоне медикаментозной иммуносупрессии развивается быстрее; у 30% пациентов через 5 лет регистрируется цирроз печеночного трансплантата, что служит показанием для выполнения ретрансплантации печени. Факторами риска быстрого прогрессирования гепатита С в печеночном трансплантате с исходом в цирроз являются:
ПВТ до и после трансплантации позволяет снизить риск прогрессирования болезни после операции. Профилактика и лечение возвратной ВГС-инфекции при трансплантации печениЦелью ПВТ в дотрансплантационном периоде является снижение вирусной нагрузки. Возможность проведения ПВТ пациентам до ТП определяется степенью компенсации функции печени и решается в индивидуальном порядке. Только 25% пациентов с циррозом печени ВГС- этиологии не имеют противопоказаний для ПВТ. В большинстве случаев у пациентов с ЦП класса В и С по шкале Чайлд-Пью от проведения ПВТ приходится отказываться ввиду наличия противопоказаний к ее проведению. Перед трансплантацией печени ПВТ стандартными дозами препаратов можно рекомендовать только при компенсации цирроза до уровня класса А по Чайлд-Пью. (предпочтительно при генотипах 2 и 3 вируса гепатита С). Иммуносупрессия, проводимая реципиенту после ТП, усиливает некровоспалительные процессы в печени, индуцированные возвратной ВГС- инфекцией. При этом у 23% пациентов в течение 3-х лет после ТП развивается цирроз печеночного трансплантата. ПВТ после ТП может начинаться еще до развития клинических признаков ОГС при морфологическом подтверждении активности процесса в печени. Препаратами выбора являются пегилированные интерфероны и рибавирин. Примерно 40% пациентов после трансплантации печени могут стать кандидатами для раннего начала ПВТ (отсутствие цитопении). Комбинация пегилированного интерферона с рибавирином позволяет добиться УВО в 9-39% случаев, при этом лучшие результаты отмечены при 2 и 3 генотипах вируса гепатита С. Многочисленные исследования свидетельствуют о большом количестве осложнений при раннем начале (1-2 мес. после операции) ПВТ, что в 50% случаев требует снижения доз интерферона и рибавирина. В связи с этим рекомендовать профилактическое назначение противовирусных препаратов после ТП в настоящее время не представляется возможным. ПВТ ВГС-инфекции в трансплантате следует начинать с 3 месяцев после операции, когда снижаются и окончательно подбираются дозы иммуносупрессивных препаратов, стабилизируется состояние пациентов. Противовирусная терапия позволяет достичь УВО менее чем у 50% пациентов. Вместе с тем она оправдана для снижения интенсивности фиброза печени. Показаниями для проведения ПВТ после ТП служат:
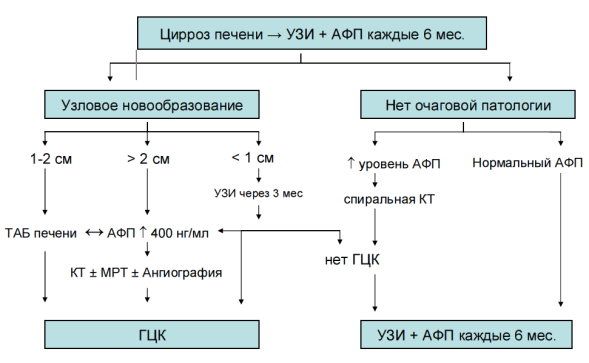
Ввиду плохой переносимости рибавирина большинством исследователей не подтверждены преимущества комбинированной терапии по сравнению с монотерапией пегилированым интерфероном в остром периоде гепатита С после ТП. Лечение следует проводить стандартными дозировками пегилированного интерферона на протяжение 24-48 недель. У 48% пациентов после ТП с легким течением гепатита С и у 19% - с тяжелым течением удается достичь УВО при комбинированной терапии пегилированным интерфероном α и рибавирином. В рандомизированных исследованиях показано, что риск развития острой клеточной реакции отторжения при назначении комбинированной ПВТ составляет от 0% до 5%. В настоящее время появились результаты первых исследованиях по применению тройной терапии с включением ингибиторов протеазы в лечение пациентов с возвратным гепатитом С после ТП. Эффективность тройной терапии у этой категории пациентов также выше. Гепатоцеллюлярная карциномаГепатоцеллюлярная карцинома во всем мире представляет собой серьезную проблему для системы здравоохранения по причине высокой заболеваемости, смертности (ежегодно в мире погибает более 1 250 000 человек) и быстрого прогрессирования. На сегодняшний день ГЦК по частоте занимает 6 место среди всех злокачественных опухолей у человека. Считается, что заболеваемость ГЦК продолжит повышаться в ближайшие десятилетия, что связано с увеличением числа больных вирусным циррозом печени и увеличением продолжительности их жизни за счет широко внедренных и в достаточной степени эффективных методов патогенетической и симптоматической терапии. Скрининг. Факторами риска развития ГЦК считаются наличие HBsAg и/или анти-ВГС, крупноузловой цирроз печени любой этиологии, мужской пол. Больным из группы риска необходимо проводить скрининговое обследование (рис. 1). Рисунок 1 . Скрининг ГЦК. Врачебная тактика (по El-Serag 2007.) ТАБ - тонкоигольная аспирационная биопсия, КТ - компьютерная томография, МРТ- магнитно-резонансная томография.
Лечение ГЦК
Стратегия предотвращения. Уменьшить заболеваемость больных ГЦК и увеличить их выживаемость можно только применяя методы первичной профилактики (вакцинация против гепатита B) и проводя противовирусное лечение больных вирусными гепатитами В и С, а также используя активный скрининг в группах риска. Обнадеживают результаты исследований, свидетельствующие об уменьшении вероятности возникновения ГЦК, связанной с ВГС в группах больных, получающих современные схемы противовирусной терапии. Лечение хронического гепатита С у больных с микст-инфекцией ВГС/ВГВ [30, 33, 34]Стратегия и тактика лечения при микст-инфекции ВГС/ВГВ окончательно не разработана. Учитывая, что пегилированный интерферон эффективен и зарегистрирован для лечения как ХГС, так и ХГВ, он рассматривается в качестве препарата первой линии у больных с сочетанной инфекцией. Тактика лечения определяется спектром выявляемых маркеров ВГВ- и ВГС-инфекции при наличии хронического гепатита сочетанной этиологии. У больных с преимущественной репликацией ВГС (РНК ВГС +, ДНК ВГВ -) или доказанной репликацией и ВГС, и ВГВ (РНК ВГС +, ДНК ВГВ +) рекомендуется лечение по программе хронического гепатита С . В ряде случаев после стойкой элиминации вируса гепатита С и прекращения лечения у первой категории больных может наблюдаться реактивация ВГВ- инфекции (вследствие устранения ингибирующего действия вируса гепатита С), данная ситуация может потребовать назначения пациенту нуклеозидных аналогов. У больных с выявлением репликативной активности только ВГВ (ДНК ВГВ +, РНК ВГС -) рекомендуется выбор препаратов разрешенных для лечения гепатита В в зависимости от результатов обследования. Адъювантная (вспомогательная) терапия ХГСПрепараты глицирризиновой кислоты (Фосфоглив). На сегодняшний день в крупном многоцентровом международном исследовании на пациентах европейской расы доказано, что препараты глицирризиновой кислоты имеют патогенетическое и клиническое обоснование для применения в качестве терапии, замедляющей прогрессирование заболевания, при ХГС у пациентов с отсутствием ответа на стандартную ПВТ или имеющих противопоказания к ее назначению [39]. Аналогичные результаты получены в процессе проведения отечественного открытого сравнительного рандомизированного исследования ОРИОН [12,17] по оценке эффективности отечественных препаратов Альтевир и Фосфоглив в комбинированной терапии больных хроническим гепатитом С. Согласно
полученным данным у пациентов с ХГС при невозможности проведения ПВТ или
при наличии противопоказаний к ПВТ может применяться фосфоглив в дозе
2,5 г внутривенно 5 раз в неделю в течение 8 недель, далее Возможны другие режимы введения препарата согласно инструкции, например, фосфоглив по 2 табл 3 раза в день перорально не менее 6 месяцев или фосфоглив форте по 1 табл 3 раза в день перорально не менее 6 мес. Силибинин (Легалон) при внутривенном введении в дозе 10 - 15 мг/кг массы тела в день может снижать вирусную кинетику и применяться в качестве адъювантного ( вспомогательного, профилактического) средства у пациентов с ХГС [35]. Адеметионин. На основании выполненного в России исследования (включено 80 пациентов) показано, что добавление перорального адеметионина (Гептрала®) в дозе 1200 мг в день к комплексной терапии ИФН α-2b и рибавирином у больных ХГС приводило к достоверно более редкому развитию психической депрессии и ее более мягкому течению, чем в группе пациентов, получавших только интерферон α-2b и рибавирин [3] (В-2) Приложение 1. Классификация степени тяжести цирроза печени по Чайлд-Пью (Сhild-Рugh)
Приложение 2. Шкала Бека оценки депрессивных проявлений (BDI-II)Инструкция: Этот вопросник состоит из 21 группы утверждений. Прочтите внимательно каждую группу, а затем выберите одно утверждение в каждой группе, наилучшим образом отражающее ваше самочувствие в течение последних двух недель, включая сегодняшний день. Обведите кружком номер рядом с выбранным вами утверждением. Если несколько утверждений в одной группе представляются вам одинаково подходящими, обведите утверждение с самым большим номером в этой группе. Проследите за тем, чтобы не выбрать больше одного утверждения для любой группы, включая группу 16 (Изменения характера сна) и группу 18 (Изменения аппетита). 1. Грусть 2. Пессимизм 3. Неудачи в прошлом 4. Утрата чувства удовольствия 5 Чувство вины 6 Чувство наказания 7 Неприязнь к себе 8
Самокритика 9
Мысли о самоубийстве или желание покончить с собой 10 Плаксивость 11 Возбудимость 12 Потеря интереса 13
Нерешительность 14 Бесполезность 15 Утрата способности к
активной деятельности 16 Изменения в характере сна 17 Раздражительность 18 Изменения аппетита 19 Снижение способности
сосредотачиваться 20 Усталость или утомляемость 21 Потеря сексуального влечения
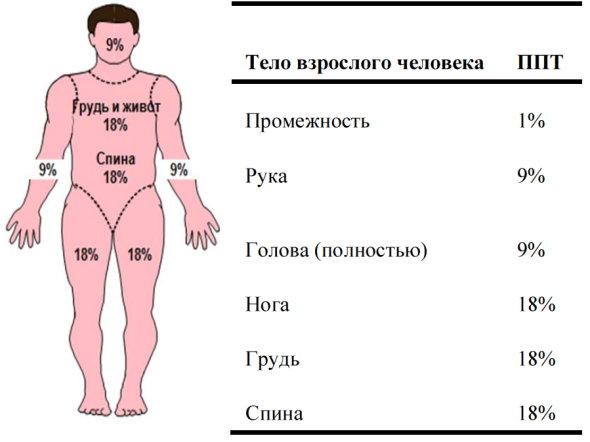
Приложение 3. Оценка площади поверхности тела (ППТ) [13]
Приложение 4 [4]Алгоритм лечения хронического гепатита С у больных с ВИЧ- инфекцией (не нуждающихся в тройной терапии). Рекомендации Европейского клинического общества по СПИДУ (EACS), версия 6.1, ноябрь 2012 г. * Если нет показаний для назначения тройной терапии (низкая
вирусная нагрузка до начала терапии, стадия фиброза 0 - 1, генотип СС
ИЛ28В
Использованная литература1. Богомолов П.О., Буеверов А.О. Эффективность и безопасность комбинированной терапии отечественными противовирусными препаратами (интераль и рибапег) хронического гепатита С // Фарматека - 2006. - №5. - С.28-32. 2. Богомолов П.О., Буеверов А.О., Дубинина
Н.В. и др. Эффективность лечения больных хроническим гепатитом С с 1-м
генотипом вируса стандартным интерфероном α// Клин. перспект.
гастроэнтерол. гепатол. 3. Буеверов А.О., Богомолов П.О., Дубинина Н.В., Мациевич М.В., Ивашкин В.Т. Гептрал® (адеметионин) в комплексной противовирусной терапии хронического гепатита С (Предварительные результаты), клин. перспект. гастроэнтерол. гепатол. 2010 №2 С. 31-36. 4. Гепатит С и ВИЧ-инфекция: тактика ведения пациентов с сочетанной инфекцией (Клинический протокол для Европейского региона ВОЗ) http://www.euro.who.int/_data/assets/pdf_file/0010/78148/HEP_C_rus.pdf 5. Дерябин П.Г., Шахгильдян И.В. «Гепатит С: фундаментальные и прикладные проблемы». В кн.: «Изучение эволюции вирусов в рамках проблемы безопасности и социально значимых инфекций».- М, 2011.-С.88- 98. 6. Ершова О.Н., Шахгильдян И.В. «Естественные пути передачи вируса гепатита С - современный взгляд на проблему». Детские инфекции, 2006, № 1, стр. 16-18. 7. Зуева Л.П., Рахманова А.Г., Колосовская Е.Н., Калинина З.П., Петрова О.Е., Дмитриева М.И./ Эпидемиологическая оценка распространенности вирусных гепатитов В и С у персонала и пациентов в стационарах С- Петербурга// Эпидемиология и инфекционные болезни, 2012, No.2, С. - 41-45 8. Ивашкин В.Т. Маевская М.В., Морозова М.А., Люсина Е.О. Современные схемы лечения хронического гепатита С, Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2012. - Т.22. - №1. - С.36-44. 9. Ивашкин В.Т., Павлов Ч.С. Фиброз печени//Монография -М.:ГЭОТАР- Медиа, 2011.-168с. 10. Ивашкин В.Т., Маевская М.В., Богомолов П.О., Никитин И.Г., Буеверов А.О., Лапшин А.В. Результаты открытого сравнительного рандомизированного исследования ОРИОН: оценка эффективности отечественных препаратов Альтевир и Фосфоглив в комбинированной терапии больных хроническим гепатитом С, Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2012. - принято в печать 11. Игнатова Т.М. Телапревир в лечении больных хроническим гепатитом С: вопросы безопасности, Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2012. - Т.22. - №4. - С.47-57. 12. Лапшин A.B., Маевская М.В., Ивашкин В.Т., Богомолов П.О., Никитин И.Г., Знойко О. О. Влияние генетических полиморфизмов гена IL28B на эффективность противовирусной терапии хронического гепатита С стандартным интерфероном-a, Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2012. -принято в печать 13. Львов Д.К., Шахгильдян И.В., Дерябин П.Г. «Гепатит С (этиология, эпидемиология, клиника, диагностика, лечение, профилактика)». В кн. «Медицинская вирусология», руководство для врачей. Москва, медицинское информационное агенство, 2008, стр.483-490. 14. Маев И.В., Казюлин A.H., Кучерявый Ю.А., Маевская Е.А. Заболевания печени(Обзор материалов Семнадцатой Российской Гастроэнтерологической Недели, 10-12 октября 2011 г., Москва), Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2012. - Т.22. - №3. - С.49-56 15. Маевская М. В. Предварительные результаты открытого сравнительного рандомизированного исследования PHG-M3/P01-09 «ОРИОН» по применению препарата «Фосфоглив» в комбинированной терапии больных хроническим гепатитом С, Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2011. - Т.21. - №4. - С.52-59. 16. Павлов Ч.С., Глушенков Д.В., Ивашкин В.Т.
Современные возможности эластометрии, фибро- и акти- теста в диагностике
фиброза печени//Российский журнал гастроэнтерологии, гепатологии,
колопроктологии № 4 , том XVIII , 2008, стр.43-52 18. Павлов Ч.С., Котович М.М. Место биопсии и морфологического исследования ткани печени у детей и взрослых в практике клинициста//Клиническая медицина, Том 85, № 9, 2007г.: Стр.72-77 19. Пименов Н.Н., Чуланов В.П., Комарова С.В. и соавт. Гепатит С в России: эпидемиологическая характеристика и пути совершенствования диагностики и надзора // Эпидемиология и инфекционные болезни - 2012. - №3. - С. 4-9. 20. Рахманова A.Г., Слепцова С.С., Жолобов В.Е. / Вакцинопрофилактика вирусного гепатита В //журнал рецензируемый ВAК <<Медико-биологические и социально-психологические проблемы безопасности в чрезвычайных ситуациях» 2012, No.3, С.56-61 21. Рахманова AX., Яковлев A.A. Хронические вирусные гепатиты и ВИЧ-инфекция Из-во <<ВВМ>> 2011-С. 164 22. Слепцова С.С., Рахманова A.R, Бугаева Т.Т., Вирусные гепатиты, как основные факторы формирования цирроза и первичного рака печени в республике Саха-Якутия, журнал рецензируемый ВАК «ВИЧ-инфекции и иммуносупрессии>> 2012, No.2, С.-109-116 23. Хазанов А.И., Плюснин С.В., Язенок Н.С.
Использование российских противовирусных препаратов в лечении
хронического гепатита С. // Российский журнал гастроэнтерологии,
гепатологии, колопроктологии. - 2005. - т. XV. - №1. - С. 32. 25. Хронические вирусные гепатиты и цирроз печени под редакцией А.Г. Рахмановой. Изд-во Спец Лит., 2006 С.-411 26. Шахгильдян И.В., Ершова О.Н., Кистенева Л.Б. и др. «Активность перинатальной передачи вируса гепатита С. Степень влияния на ее интенсивность отдельных факторов». Материалы ХVI Конгресса педиатров России с международным участием. Москва, 2012, стр. 851-853. 27. Шахгильдян И.В., Ершова О.Н., Михайлов М.И. и др. «Современная характеристика острого и хронического гепатита С в России». Материалы международного симпозиума. Брест, 2011, стр.184-186. 28. Шахгильдян И.В., Михайлов М.И., Онищенко Г.Г. «Парентеральные вирусные гепатиты (эпидемиология, диагностика, профилактика)». Москва, ГОУ ВЦНМУ МЗ РФ, 2003. - 380 стр. 29. Ющук Н.Д., Максимов С.Л., Иванова Л.М., Климова Е.А., Знойко О. О., Кравченко А.В., Комбинированная терапия хронического гепатита С пегилированным интерфероном а-2а и рибавирином у больных с ВИЧ- инфекцией и больных с моноинфекцией HCV, Российский журнал гастроэнтерологии, гепатологии, колопроктологии, - 2009. - Т.19. - №1. - С.35-42 30. Ющук Н.Д., Климова Е.А., Знойко О.О. и др. Протокол диагностики и лечения больных вирусными гепатитами В и С // Рос. журн. гастроэнтерол. гепатол. колопроктол. - 2010. - Т. 20, № 6. - С. 4-60. 31. Яковлев А.А., Виноградова Е.Н., Рахманова А.Г., Хронические вирусные гепатиты СПб Из-во НИИХ СПб ГУ - 287 с. 32. Boursier J., de Ledinghen V., Zarski J.P. et al. Comparison of eight diagnostic algorithms for liver fibrosis in hepatitis C: new algorithms are more precise and entirely noninvasive. Hepatology. 2012 Jan;55(1):58-67 33. EASL Clinical Practice Guidelines: Management of hepatitis C virus infection, Journal of Hepatology 2011 vol. 55, 245-264 34. Ghany M, Nelson D, Strader D, Thomas D, Seeff L An Update on Treatment of Genotype 1 Chronic Hepatitis C Virus Infection: 2011 Practice Guideline by the American Association for the Study of Liver Diseases, Hepatology, Vol.54, No. 4, 2011, 1433-1444 35. Guedj J, Daharl H, Pohl R, Ferenci P, Perelson A Understanding silibinin’s modes of action against HCV using viral kinetic modelingJournal of Hepatology Volume 56, Issue 5 , Pages 1019-1024, May 2012 36. INCIVO Summary of Product Characteristics 37. Jacobson IM, McHutchinson J, Dusheiko G, Di Bisceglie AM, Reddy KR, et al. (2011) Telaprevir for previously untreated chronic Hepatitis C Virus Infection. N Engl J Med. 364;25, 2405-2416. 38. Jordan J. Feld, MD, MPH, Hemant Shah, MD, MScCH HPTE, inPractice® Hepatology 1-8 Management of Hepatitis C Infection http://www.clinicaloptions.com/inPractice/Hepatology/Hepatology/ch8_Mgmt_of_ Hep_C_Infection.aspx 39. Manns MP, Wedemeyer H, Singer A, Khomutjanskaja N, Dienes HP, Roskams T, Goldin R, Hehnke U, Inoue H; the European SNMC Study GroupGlycyrrhizin in patients who failed previous interferon alpha-based therapies: biochemical and histological effects after 52 weeks.J Viral Hepat. 2012 Aug;19(8):537-546. doi: 10.1111/j.1365-2893.2011.01579.x. Epub 2012 Feb 24. 40. Sarrazin C, Christophe Hezode Ch, Zeuzem S, Jean-Michel Pawlotsky J- M Antiviral strategies in hepatitis C virus infection Journal of Hepatology 2012, S88-S100 41. Sherman KE, et al. Response-guided telaprevir combination treatment for hepatitis C virus infection. N Engl J Med 2011;365:1014-24. Erratum in: N Engl J Med 2011;365:1551. 42. Zarski J.P., Sturm N., Guechot J. et al. Comparison of nine blood tests and transient elastography for liver fibrosis in chronic hepatitis C: the ANRS HCEP-23 study. J Hepatol. 2012 Jan;56(1):55-62. 43. Zeuzem S et al. Telaprevir for Retreatment of HCV Infection. N Engl J Med 2011;364:241728.
Реклама |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
В вашем здоровье заинтересованы только вы сами… |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||